Yuanfeng POV: Aktualisierte EUDAMED-Zeitleiste
Die EU-Kommission hat kürzlich Aktualisierungen für die Fertigstellung und Umsetzung von EUDAMED auf der Grundlage der Änderung 2024/1860 angekündigt.Dieser Artikel beschreibt die derzeitigen EUDAMED-Zeitpläne und unsere Sichtweise auf diese Zeitpläne, um der Industrie zu helfen, sich entsprechend vorzubereiten..
Aktuelle EUDAMED-Zeitpläne:
- Der Zieldatum für die erste obligatorische Anwendung der funktionellen EUDAMED-Module ist weiterhin der 1. Januar 2026.Das Vigilance-Modul wird voraussichtlich ab dem dritten Quartal 2026 obligatorisch sein, wobei die vollständige EUDAMED-Funktionalität für das zweite Quartal 2027 geplant ist..
- Die Module Akteur, UDI und Geräte, Zertifikate und Marktüberwachung werden derzeit geprüft.Die unabhängige Prüfung des minimalen lebensfähigen Produkts (MVP) soll die Funktionalität und die Vernetzung der Module, die als auditbereit eingestuft werden, bewerten und bestätigen.Dieses Audit soll bis zum zweiten Quartal 2025 abgeschlossen sein.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Es wird erwartet, dass die Module für Akteur, UDI und Geräte, Zertifikate und Marktüberwachung Ende des zweiten Quartals 2025 voll funktionsfähig erklärt werden, was zu ihrem obligatorischen Anwendungsdatum am 1. Januar führt. 2026.
- Ich weiß. - Es wird erwartet, dass die Module Akteur, UDI und Geräte, Zertifikate und Marktüberwachung bis Ende des zweiten Quartals 2025 voll funktionsfähig erklärt und am 1. Januar 2026 für den Einsatz in der Industrie vorgeschrieben werden.
- Das Vigilance-Modul ist nicht Teil des laufenden MVP-Audits und wird nicht zusammen mit den zuvor genannten Modulen für voll funktionsfähig erklärt.Der überarbeitete Zeitplan zeigt, dass die Prüfung dieses Moduls zwischen dem zweiten und dritten Quartal 2025 stattfinden wird., mit dem Ziel, dass die obligatorische Anwendung im zweiten Quartal 2026 beginnt.
- Ich weiß. - Die Entwicklung des Moduls "Klinische Untersuchungen/Leistungsstudien" (CI/PS) soll bis zum dritten Quartal 2026 fortgesetzt werden.Ein Audit zur Bewertung des CI/PS-Moduls zusammen mit den anderen fünf (5) Modulen wird abgeschlossen, sobald das CI/PS-MVP entwickelt wurde.
- Ich weiß.
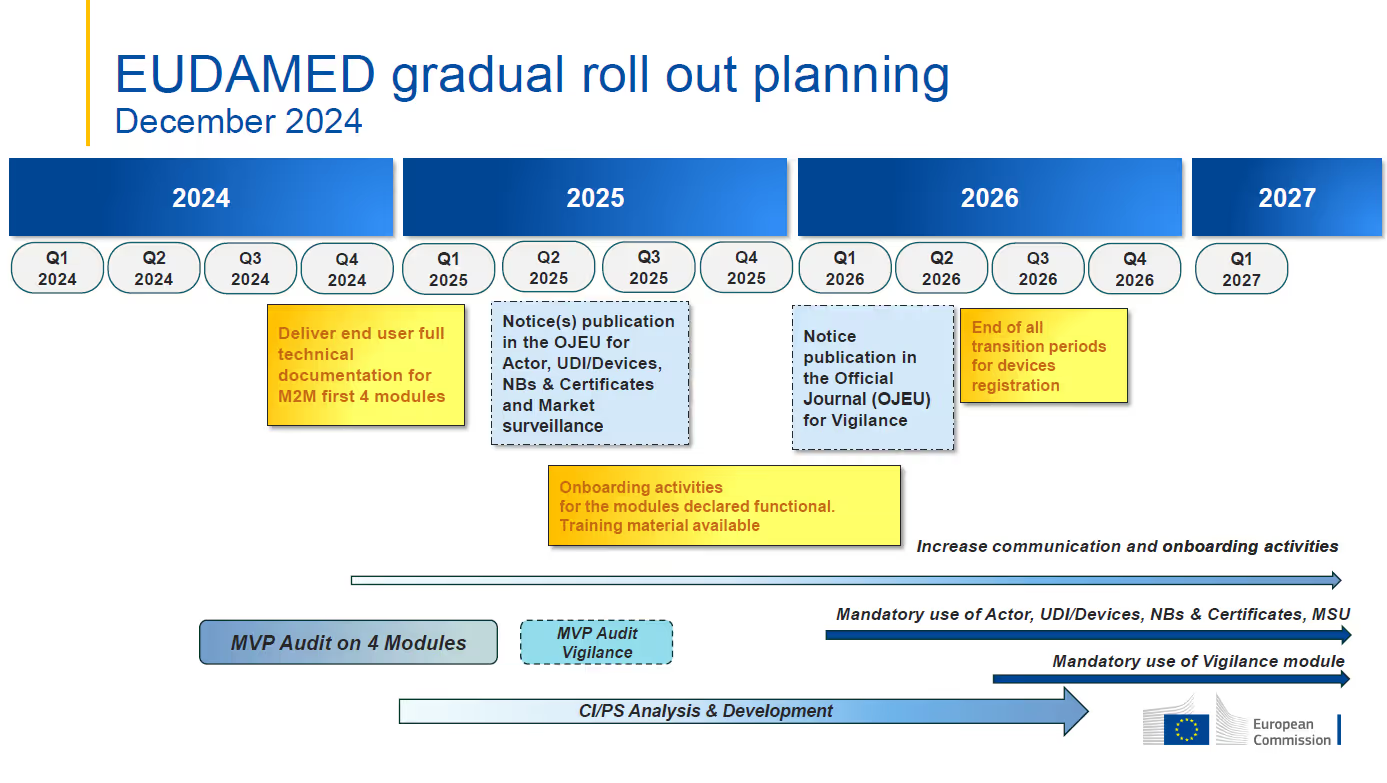
Foto mit Genehmigung desEuropäische Kommission
Die EU-Kommission hat kürzlich Aktualisierungen für die Fertigstellung und Umsetzung von EUDAMED auf der Grundlage vonÄnderung 2024/1860.Dieser Artikel beschreibt die derzeitigen EUDAMED-Zeitpläne und unsere Sichtweise auf diese Zeitpläne, um der Industrie zu helfen, sich entsprechend vorzubereiten.
Aktuelle EUDAMED-Zeitpläne:
- Der Zieldatum für die erste obligatorische Anwendung der funktionellen EUDAMED-Module ist weiterhin der 1. Januar 2026.Das Vigilance-Modul wird voraussichtlich ab dem dritten Quartal 2026 obligatorisch sein, wobei die vollständige EUDAMED-Funktionalität für das zweite Quartal 2027 geplant ist..
- Die Module Akteur, UDI und Geräte, Zertifikate und Marktüberwachung werden derzeit geprüft.Die unabhängige Prüfung des minimalen lebensfähigen Produkts (MVP) soll die Funktionalität und die Vernetzung der Module, die als auditbereit eingestuft werden, bewerten und bestätigen.Dieses Audit soll bis zum zweiten Quartal 2025 abgeschlossen sein.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Es wird erwartet, dass die Module für Akteur, UDI und Geräte, Zertifikate und Marktüberwachung Ende des zweiten Quartals 2025 voll funktionsfähig erklärt werden, was zu ihrem obligatorischen Anwendungsdatum am 1. Januar führt. 2026.
- Ich weiß. - Es wird erwartet, dass die Module Akteur, UDI und Geräte, Zertifikate und Marktüberwachung bis Ende des zweiten Quartals 2025 voll funktionsfähig erklärt und am 1. Januar 2026 für den Einsatz in der Industrie vorgeschrieben werden.
- Das Vigilance-Modul ist nicht Teil des laufenden MVP-Audits und wird nicht zusammen mit den zuvor genannten Modulen für voll funktionsfähig erklärt.Der überarbeitete Zeitplan zeigt, dass die Prüfung dieses Moduls zwischen dem zweiten und dritten Quartal 2025 stattfinden wird., mit dem Ziel, dass die obligatorische Anwendung im zweiten Quartal 2026 beginnt.
- Ich weiß. - Die Entwicklung des Moduls "Klinische Untersuchungen/Leistungsstudien" (CI/PS) soll bis zum dritten Quartal 2026 fortgesetzt werden.Ein Audit zur Bewertung des CI/PS-Moduls zusammen mit den anderen fünf (5) Modulen wird abgeschlossen, sobald das CI/PS-MVP entwickelt wurde.
- Ich weiß.

Foto mit Genehmigung desEuropäische Kommission
Wie Rimsys die Auswirkungen dieser Ankündigung für die einzelnen Interessengruppen sieht:
Yuanfeng
Die UDI steht im Vordergrund, ebenso wie die zukünftige Interaktion mit dem Vigilance-Modul.Da Rimsys die UDI- und die Marktüberwachungsfunktion unabhängig von den aktualisierten Zielterminen weiterentwickeln wird,Wir erkennen auch die möglichen Auswirkungen der Einrichtung von Datenübertragungsmöglichkeiten (DTX) zur Interaktion mit EUDAMED in einer Maschine-zu-Maschine-Kapazität (M2M) an.Mit der Veröffentlichung der endgültigen Anforderungen für M2M DTX an EUDAMED, ist Rimsys in der Lage, unsere Verbindung abzuschließen und M2M-Fähigkeiten als Teil der EUDAMED-Lösung bereitzustellen.
Industriezweig/Kunde
Da die Europäische Kommission (EK) die EUDAMED-Zeitpläne mehrfach aktualisiert hat, erwarten wir, dass die Industrie etwas zurückhaltend ist, die neuen Zieltermine zu akzeptieren.Dies könnte die Wiedereingliederung in die EUDAMED-Vorbereitungen verzögern.Wir erwarten jedoch nicht, daß die EG diese aktualisierten Zeitpläne verschiebt.Hersteller, die nicht vorhaben, EUDAMED bis zum zweiten Quartal dieses Jahres Daten einzureichen, sollten mit erheblichen Herausforderungen rechnen, um diese Fristen zu erfüllen.Mit dem laufenden Audit der erwarteten Module und der damit verbundenen veröffentlichten technischen DokumentationRimsys empfiehlt, Schritte zu unternehmen, um die Regulierungsdaten jetzt zu organisieren und ihre Informationen frühzeitig in alle verfügbaren EUDAMED-Module einzureichen.
Europäische Kommission
Die EG empfiehlt der Industrie dringend, ihre Lösung weiter zu entwickeln und Daten freiwillig einzureichen.Die Kommission vertritt die Auffassung, dass eine frühzeitige Übermittlung von Daten den Unternehmen einen Vorteil verschafft, indem ihre Daten vor dem Ansturm der gesamten medizinischen Industrie vorliegen.Diese Unternehmen werden auch an vorderster Front stehen, um mit den Kommissionsressourcen zu arbeiten, wenn Probleme mit der Datenübermittlung auftreten.
* Hinweis: Dieser Artikel enthält rechtliche Auslegungen und Stellungnahmen derYuanfengWir versuchen, so informativ wie möglich zu sein, aber diese Informationen sollen nicht als Ersatz für die offiziellen Leitlinien der Regulierungsbehörden dienen.

